コンテンツ
主な違い
アクチンとミオシンの主な違いは、アクチンタンパク質が筋肉や他の細胞の収縮特性の主要なサプライヤーであるのに対し、ミオシンはモーターとして働き、ミオシンフィラメントが移動するようにアデノシン三リン酸(ATP)を加水分解してエネルギーを放出することですアクチンフィラメントに沿って、2本の糸が互いにスライドするように開始します。
アクチンvs.ミオシン
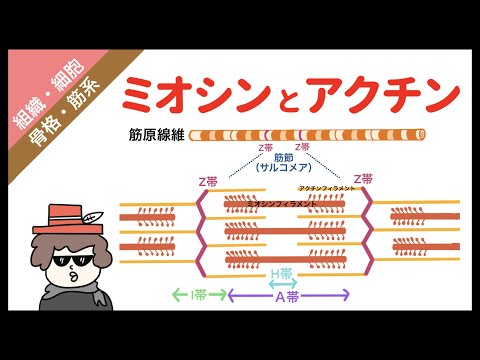
アクチンとミオシンの両方は、筋肉の収縮と細胞内運動において物理的および酵素的役割を果たす。ミオシンはサルコメアのAバンドに存在するのに対し、アクチンはAバンドとIバンドの両方に存在します。アクチンには細い(0.005 mn)、しかし短い(2 -2.6 mn)フィラメントが含まれているのに対し、ミオシンには厚い(0.01 mn)が長い(4.5 mn)フィラメントが含まれています。アクチンにはクロスブリッジはなく、滑らかな表面に存在しますが、ミオシンには粗い表面に存在するクロスブリッジが存在します。アクチンはミオシンフィラメントよりも多く、6個が各ミオシンフィラメントを囲んでいますが、ミオシンはアクチンフィラメントよりも数が少なくなっています。アクチンフィラメントは一方の端で自由であり、他方でミオシンフィラメントが両端で開いている一方、もう一方の端でZ線に結合します。アクチンはアクチン、トロポミオシン、トロポニンなどの3つのタンパク質で構成され、ミオシンはミオシンとメロミオシンなどの2つのタンパク質で構成されています。アクチンフィラメントは筋肉収縮時にHゾーンに滑り込みますが、ミオシンは筋肉収縮時に滑りません。
比較表
| アクチン | ミオシン |
| 筋肉細胞で細い収縮鎖を形成するタンパク質 | 筋肉細胞で太い収縮鎖を形成するタンパク質 |
| フィラメントのサイズ | |
| 細い(0.005μm)、および短い(2 – 2.6μm)フィラメント | 太い(0.01μm)、および長い(4.5μm)フィラメント |
| ロケーション | |
| AおよびIバンドに参加 | サルコメアのAバンドに登場。 |
| 調節タンパク質 | |
| トロポミオシンとトロポニン | メロミオシン |
| 表面 | |
| なめらか | ラフ |
| クロスブリッジ | |
| クロスブリッジは存在しません | クロスブリッジが存在します |
| 数 | |
| 数が多い | 6本のアクチンフィラメントごとに1本のミオシンフィラメントが生じます。 |
| スライディング | |
| 収縮中にHゾーンにスライドします | 収縮中にスライドしないでください |
| 終了 | |
| 片端無料 | 両端無料 |
アクチンとは?
アクチンは、筋肉細胞で細い収縮性フィラメントを形成するタンパク質について議論しています。真核細胞で最も豊富なタンパク質です。アクチンは信じられないほどタンパク質を保存しています。アクチンの2つの形態は単量体と糸状です。物理的条件下では、ATPからのエネルギーを使用して、モノマーが容易に重合してフィラメントを形成します。アクチンフィラメントの重合は、フィラメントの両端から始まります。重合の比率は両端で等しくないため、フィラメントに固有の極性が生じます。トロポミオシンとトロポニンの関係は、アクチンフィラメントを安定化します。細胞の性質と動きは、アクチンフィラメントに依存しています。アクチンフィラメントの中心的な役割は、細胞の活性な細胞骨格を形成することです。細胞骨格は物理的なサポートを提供し、細胞を周囲にリンクします。アクチンフィラメントは、細胞の運動性を助ける糸状仮足とLamellipodiaの開発に関与しています。アクチンフィラメントは、有糸分裂中の娘細胞への細胞小器官の輸送を助けます。筋肉細胞内の細いフィラメントの化合物は力を生成し、筋肉の収縮をサポートします。
ミオシンとは?
ミオシンは、筋肉細胞で太い収縮性フィラメントを形成するタンパク質について議論しています。ミオシンは、筋肉の収縮と細胞内運動に物理的および酵素的役割を果たします。すべてのミオシン分子は、1つまたは2つの重鎖と多くの軽鎖として構成されています。このタンパク質では、頭、首、尾の3つのドメインを特定できます。頭部は円形で、アクチンとATP結合部位を含んでいます。ネック領域は、α-ヘリカルを含む。尾には、太いフィラメントのシャフトからの約300のミオシン分子が含まれています。ミオシンは、アクチンを固定し、ATPを加水分解するタンパク質のスーパーファミリーであり、ほとんどが筋肉細胞に位置しています。これらの分子のミオシン頭部は、手rowぎボートのパドルのように細いフィラメントに向かって外側に発達します。テール部位は、異なる分子の結合部位を含みます。ミオシンには18のクラスがあります。 13種類のミオシンがミオシンI、II、III、IVなどとして識別できます。ミオシンIは小胞の輸送に関与します。ミオシンIIは筋肉の収縮に関与しています。筋肉の収縮は、スライディングフィラメント理論として説明されています。細いアクチンフィラメントは太いミオシンフィラメントの上を滑って、筋肉に緊張をもたらします。各ミオシンの太いフィラメントは細いアクチンフィラメントで囲まれ、各細いフィラメントは太いフィラメントで囲まれています。これらのフィラメント束の多くは、筋肉細胞の機能部分を構成しています。
主な違い
- アクチンは、ヒトの筋肉で細い収縮フィラメントを形成するタンパク質を指し、ミオシンは筋肉細胞で太い収縮フィラメントを形成するタンパク質を指します。
- アクチンは細い(0.005μm)、短い(2 – 2.6μm)フィラメントを作りますが、ミオシンは太い(0.01μm)、長い(4.5μm)フィラメントを作ります。
- アクチンフィラメントはトロポミオシンとトロポニンから成り、ミオシンフィラメントはメロミオシンから成ります。
- アクチンフィラメントはAおよびIバンドに存在しますが、逆にミオシンフィラメントはサルコメアのAバンドに存在します。
- アクチンフィラメントは架橋を形成しませんが、ミオシンフィラメントは架橋を形成します。
- アクチンフィラメントの外側は滑らかですが、ミオシンフィラメントの表面は粗いです。
- アクチンフィラメントは多数ありますが、6つのアクチンフィラメントごとに1つのミオシンフィラメントが発生します。
- ミオシンフィラメントは両端が自由ですが、アクチンフィラメントは一端が自由です。
- アクチンフィラメントは収縮時にHゾーンに滑り込みますが、ミオシンフィラメントは収縮時に滑りません。
結論
この議論の上で、アクチンとミオシンは筋肉細胞で収縮性フィラメントを形成する2種類のタンパク質であると結論付けられます。アクチンは細くて短いフィラメントを作り、ミオシンは太くて長いフィラメントを作ります。アクチンとミオシンの両方が真核細胞に存在し、細胞骨格を形成し、分子の動きに関与しています。


